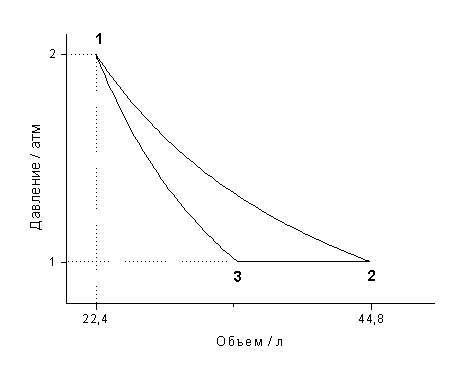
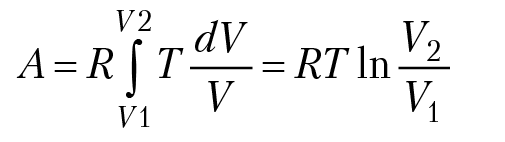Как изменится внутренняя энергия идеального газа при изобарном расширении
Внутренняя энергия тела термодинамической системы может меняться при совершении работы и в процессе теплопередачи. Закон сохранения и превращения энергии, распространённый на тепловые явления, называется первым законом термодинамики первым началом термодинамики и записывается в виде. Найдём значение молярной теплоёмкости при постоянном объёме у одноатомного идеального газа. Интересно заметить, что молярная теплоёмкость при постоянном объёме у всех одноатомных идеальных газов получилась одна и та же:. Удельные же теплоёмкости у всех одноатомных идеальных газов различные и зависят от молярной массы.


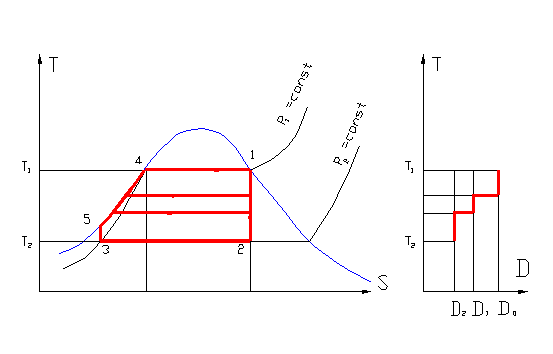



Статистический метод основан на представлении о том, что все вещества состоят из молекул, находящихся в хаотическом движении. Так как число молекул огромно, то можно, применяя законы статистики, найти определённые закономерности для всего вещества в целом. Термодинамический метод исходит из основных опытных законов, получивших название законов термодинамики. Термодинамический метод подходит к изучению явлений подобно классической механике, которая базируется на опытных законах Ньютона. При таком подходе не рассматривается внутреннее строение вещества. Идеальный газ — теоретическая модель газа, для которого можно пренебречь размерами молекул, силами молекулярного взаимодействия; соударения молекул в таком газе происходят по закону соударения упругих шаров.
- Термодинамика. Идеальный газ. Законы идеального газа - презентация онлайн
- С нами работают преподавателей из областей знаний. Мы публикуем только качественные материалы.
- Помочь проекту. Системой называется совокупность рассматриваемых тел частиц , которые могут взаимодействовать между собой и с другими телами внешней средой посредством обмена веществом и энергией.
- Термодин а мика, наука о наиболее общих свойствах макроскопических систем, находящихся в состоянии термодинамического равновесия, и о процессах перехода между этими состояниями.
- Энергетическое образование
- Внутренняя энергия идеального газа является одной из основных характеристик вещества, определяющей его термодинамические свойства.
- Термодинамика фотонного газа рассматривает электромагнитное излучение , используя понятия и методы термодинамики.
- В этой модели, во-первых, предполагается, что составляющие газ частицы не взаимодействуют друг с другом, то есть их размеры пренебрежимо малы, поэтому в объёме , занятом идеальным газом, нет взаимных неупругих столкновений частиц. Частицы идеального газа претерпевают столкновения только со стенками сосуда.


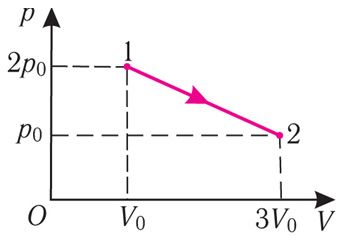


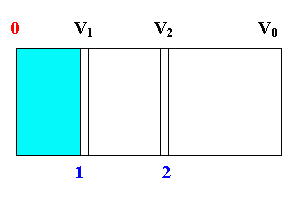
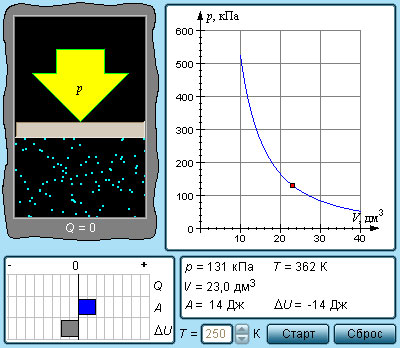
Идеальный газ - математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. В реальных условиях указанные ограничения практически не выполняются.